- ĐẠI CƯƠNG
Ung thư gan gồm các ung thư nguyên phát và thứ phát.
– Ung thư gan nguyên phát phần lớn là ung thư tế bào gan (hepatocellular carcinoma – HCC) hoặc tế bào ống mật (cholangio carcinoma), còn ung thư gan thứ phát là do di căn từ ung thư ở nơi khác đến gan. Trong bài này chủ yếu nói về ung thư nguyên phát của gan.
– Ung thư gan nguyên phát thường gặp ở các nước nhiệt đới. Ở Việt Nam, ung thư gan đứng hàng thứ ba sau ung thư phế quản và ung thư dạ dày, hay gặp nhất là ung thư tế bào gan.
- NGUYÊN NHÂN ĐIỀU KIỆN THUẬN LỢI
Nguyên nhân trực tiếp gây ung thư gan chưa rõ ràng, cơ chế gây ung thư được cho là do rối loạn cấu trúc AND của nhân tế bào. Có nhiều yếu tố nguy cơ có thể làm rối loạn cấu trúc gây đột biến gen như:
2.1.Viêm gan vi rút
Có sự liên quan giữa viêm gan vi rut B và C với ung thư gan nguyên phát. Ở Việt Nam, 81% bệnh nhân ung thư gan có kháng nguyên HBsAg (+) (viêm gan B) so với nhóm bệnh thường là 15%. Theo H.H. Hann (2004), 60% ung thư tế bào gan (HCC) có liên quan tới viêm gan B và 25% có liên quan đến viêm gan C.
2.2. Xơ gan
Ung thư gan thường gặp ở bệnh nhân xơ gan. Ở Việt Nam, 52 – 80% số bệnh nhân ung thư gan có xơ gan (tỷ lệ này ở Đức là 50% và ở Mỹ là 89%), trong đó đa số là xơ gan do rượu.
2.3. Các chất gây hoại tử tế bào gan và xơ gan
– Nấm mốc Aflatoxin từ lạc, đỗ mốc.
– Chất độc: nhất là chất độc màu da cam (dioxin) làm rụng lá cây. Tetraclorua carbon, các chất màu Azo hoặc nitrosamin gây ung thư gan trên thực nghiệm.
2.4. Chế độ ăn uống
Thức ăn bị mốc, uống rượu nhiều, chế độ ăn ít đạm, nhiều mỡ, ít sinh tố B1.
III. GIẢI PHẪU BỆNH LÝ
3.1. Đại thể
– Khối ung thư màu vàng nhạt hoặc trắng nổi gồ trên bề mặt gan, có ranh giới tương đối rõ, xung quanh có nhiều mạch máu trên nền tổ chức gan xơ hoặc bệnh thường.
– Có 3 hình thái: ung thư thể khối (thường khu trú tại một phần gan và trên nền gan không xơ), ung thư thể nhân (thường nằm rải rác và trên nền gan xơ, tiến triển nhanh), ung thư thể lan toả (như hạt kê, nằm khu trú hoặc rải rác, trên nền gan xơ, tiên lượng xấu).
3.2. Vi thể
Hay gặp nhất là ung thư tế bào gan (HCC) 89%, ung thư tế bào ống mật 3,5%. Ung thư tổ chức liên kết của gan (sarcoma) chỉ chiếm khoảng 1,5%, còn lại hỗn hợp ung thư liên bào gan và liên bào ống mật là 6%.
- CHẨN ĐOÁN
Bệnh có thể gặp ở mọi lứa tuổi (thường từ 30 – 50 tuổi), hay gặp ở nam giới.
4.1. Lâm sàng
Các triệu chứng nghèo nàn, rất khó chẩn đoán sớm nếu không có các phương tiện chẩn đoán hình ảnh hiện đại. Khi các triệu chứng rõ thường ở giai đoạn muộn, tiên lượng nặng.
4.1.1. Triệu chứng cơ năng và toàn thân
– Đau tức vùng gan liên tục.
– Chán ăn, mệt mỏi.
– Gầy sút cân nhanh.
– Đôi khi có sốt nhẹ, chỉ sốt cao khi khối u hoại tử hoặc áp xe hóa.
– Có thể gặp vàng da nhẹ do suy gan hoặc khối u làm tắc mật.
4.1.2. Triệu chứng thực thể
– Gan to, mật độ rắn chắc, bề mặt lổn nhổn không đều, ấn tức không đau, di động, u to nhanh đôi khi nghe thấy tiếng thổi tâm thu trên khối u (11 – 29%).
– Ở giai đoạn muộn có thể gặp:
+ Cổ chướng (20 – 40%): dịch thường lẫn máu.
– Lách to, tuần hoàn bàng hệ, bụng chướng, vàng da.
4.1.3. Thể lâm sàng
– Thể có khối u: khối u gan với đặc điềm nêu trên là triệu chứng đầu tiên và nổi bật.
– Thể giống như áp xe gan: gan to, đau và hội chứng nhiễm khuẩn toàn thân.
– Thể giống như xơ gan:
+ Có thể đó có một xơ gan từ trước, hoặc hội chứng xơ gan mất bù.
+ Gan to, cổ trướng, tuần hoàn bàng hệ.
– Thể chảy máu trong: khối ung thư bị vỡ do bị hoại tử gây hội chứng chảy máu trong.
– Thể hội chứng tăng áp lực tĩnh mạch cửa: lách to, cổ trướng, tuần hoàn bàng hệ, nôn ra máu.
– Thể hôn mê hạ đường huyết: hiếm gặp, có thể do ung thư bài tiết ra một chất tương tự insulin.
4.2. Cận lâm sàng
4.2.1. Xét nghiệm máu
– Hồng cầu giảm nhẹ, huyết sắc tố giảm.
– Bạch cầu và công thức bạch cầu bệnh thường (chẩn đoán phân biệt với các bệnh viêm nhiễm của gan).
– Protein giảm, tỷ lệ A/G < l.
– Bilirubin máu có thể tăng.
– Transaminase tăng vừa.
– Glucose máu thấp (do giảm tổng hợp và dự trữ glycogen hoặc u có chứa chất tương tự insulin).
– Men arginasa trong tổ chức gan giảm < 40 đơn vị (bệnh thường là > 120 đơn vị/gam tổ chức).
– Men LDH (lactico dehydrogenaza): tỷ lệ LDH5/LDH1 > l (bệnh thường < l).
4.2.2. Xét nghiệm miễn dịch (có ý nghĩa chẩn đoán)
– Xét nghiệm Alpha – Foetoprotein (AFP) là một xét nghiệm đặc hiệu. AFP là một glucoprotein thường chỉ có trong thời kỳ bào thai. Trong ung thư gan nguyên phát gặp tỷ lệ AFP (+) từ 60 – 90%. Đối với ung thư gan thứ phát xét nghiệm này âm tính. Khi AFP định lượng (> 20 ng/ml được coi là dương tính) > 400 ng/ml thì có giá trị chẩn đoán xác định là ung thư tế bào gan. Xét nghiệm AFP còn được dùng để theo dõi và đánh giá kết quả điều trị.
– Phản ứng Mantoux: thường âm tính do miễn dịch cơ thể giảm. Theo Tôn Thất Tùng: tỷ lệ âm tính là 58,7% và tiên lượng bệnh khi âm tính xấu hơn dương tính.
4.2.3. Chẩn đoán hình ảnh
– Siêu âm gan: là phương pháp chẩn đoán hình ảnh hàng đầu trong chẩn đoán ung thư gan, được áp dụng nhiều, cho tỷ lệ chẩn đoán chính xác cao. Siêu âm cho biết kích thước và vị trí u (khối u có âm vang tăng). Siêu âm còn giúp hướng dẫn cho các biện pháp điều trị ung thư gan (cắt gan, tiêm diệt u qua da). Tuy nhiên, siêu âm không cho biết bản chất khối u. Siêu âm Doppler giúp đánh giá sự xâm lấn vào tĩnh mạch cửa, tĩnh mạch trên gan và tĩnh mạch chủ dưới.
– Chụp cắt lớp vi tính (CT scaner), nhất là chụp cắt lớp vi tính có tiêm cản quang: có giá trị chẩn đoán rất sớm, 94% phát hiện được những u có đường kính > 3 cm và xác định rõ ràng vị trí u. Đây là phương pháp tốt để chẩn đoán ung thư gan.
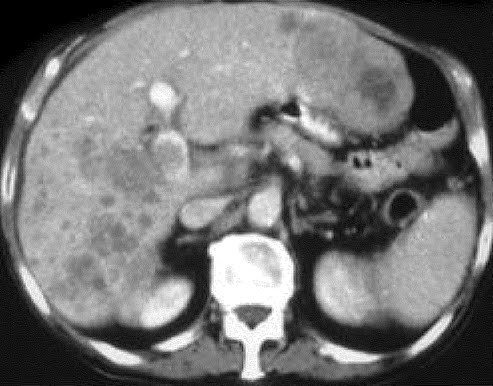
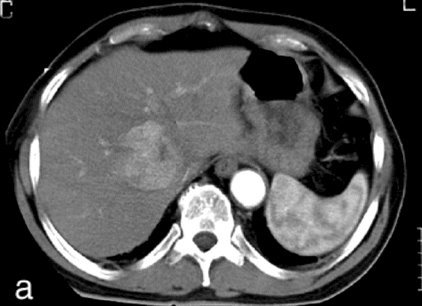
Hình ảnh của HCC trên CT (hai BN khác nhau): A-trước khi bơm thuốc cản quang: khối u đa ổ và giảm đậm độ, B-thì động mạch: khối u tăng quang rõ, trong lòng có những vùng hoại tử (giảm đậm độ và không tăng quang).
– Chụp động mạch gan chọn lọc: thấy các động mạch trong gan bị khối u đẩy rộng ra và hình ảnh đặc hiệu của ung thư gan là “hồ máu” do các động tĩnh mạch giãn rộng để làm chậm lưu lượng tuần hoàn qua vùng ung thư. Hiện nay, sử dụng chụp mạch máu số hóa xóa nền (DSA) cho thấy động mạch gan nuôi khối u giãn to, tăng tốc độ dòng chảy so với các nhánh khác của gan, khối u tăng sinh mạch rõ rệt so với nhu mô gan lành. Phương pháp này cho phép chẩn đoán đúng từ 80 – 90% các khối u < 3 cm.
– Chụp cộng hưởng từ hạt nhân (MRI): có độ chẩn đoán chính xác cao (đạt tỷ lệ chẩn đoán chính xác tới 97,5% với các u > 2 cm) và nhất là giúp phát hiện tổn thương xâm lấn tĩnh mạch trên gan.
– Chụp gan xa không chuẩn bị: thấy bóng gan to, ít thấy phản ứng màng phổi, có thể thấy hình ảnh vòm hoành cao.
– Chụp X quang lồng ngực: có thể phát hiện thấy di căn phổi.
– Chụp tĩnh mạch cửa: thấy vùng gan không ngấm thuốc (vô mạch), có hình khuyết cắt cụt, song không biết bản chất khối u.
– Chụp nhấp nháy gan: dùng phúng xạ 131I, 198Au (gắn Lên tế bào Kufer) hoặc 75 Se (gắn Lên tế bào ung thư gan) cho phép phát hiện u gan kích thước từ 2 – 3 cm trở lên (cho thấy hình khuyết), song khó phân biệt các nhân xơ gan với các nhân ung thư. Phương pháp ghi hình cắt lớp bằng bức xạ photon đơn, kỹ thuật sử dụng kháng thể đơn dòng giúp chẩn đoán ung thư gan với độ nhạy và độ đặc hiệu cao hơn.
4.2.4. Các phương pháp khác
– Soi ổ bụng: có thể đánh giá được kích thước, nhân trực tiếp các u trên bề mặt gan.
– Chọc sinh thiết gan: nhằm xét nghiệm mô bệnh học, nhất là khi nghi ngờ giữa ung thư và áp xe gan. Chọc sinh thiết gan với hướng dẫn của siêu âm giúp tiến hành kỹ thuật thuận lợi, ít tai biến và tỷ lệ chẩn đoán chính xác cao. Có thể tiến hành chọc sinh thiết gan qua nội soi ổ bụng hoặc dưới hướng dẫn của chụp cắt lớp vi tính. Tỷ lệ chẩn đoán đúng 90%.
4.3. Chẩn đoán xác định
4.3.1. Chẩn đoán xác định
Dựa vào các triệu chứng sau:
– Xét nghiệm AFP (+), nếu định lượng AFP > 400 ng/ml + CLVT khối u gan có hình ảnh ngấm thuốc đặc trưng của ung thư gan thì chẩn đoán xác định là ung thư tế bào gan.
– Siêu âm gan, chụp CT và MRI gan, chọc sinh thiết gan.
– Những người có nguy cơ cao: viêm gan virus, xơ gan…
4.3.2. Chẩn đoán phân biệt
○ Áp xe gan
Sốt cao, gan to, đau (tam chứng Fontan), bạch cầu và máu lắng tăng, phản ứng miễn dịch huỳnh quang (+), AFP (-), siêu âm có hình ổ loãng âm, chọc dò có mủ socola, điều trị bằng emetine có đỡ.
○ U lành tính của gan
– U máu (hemangiome) là u gan lành tính thường gặp nhất. Hình ảnh siêu âm là hình tăng âm, phát hiện rõ hơn khi chụp cắt lớp có tiêm thuốc cản quang. Thường chỉ điều trị phẫu thuật hoặc làm nút mạch khi có triệu chứng lâm sàng.
– Nang gan: thường chỉ có biểu hiện triệu chứng khi nang lớn hoặc có biến chứng (vỡ, nhiễm trựng, chảy máu). Khi đó điều trị chủ yếu bằng phẫu thuật nội soi cắt chỏm nang.
– Các u khác: xơ gan phì đại, adenome…
- ĐIỀU TRỊ
Có rất nhiều phương pháp điều trị UTG, bao gồm 3 nhóm chính:
– Điều trị triệt căn: cắt gan, ghép gan, đốt sóng cao tần.
– Điều trị phụ trợ: nút ĐMG, hóa chất toàn thân (sorafenib).
– Điều trị triệu chứng: giảm đau, chống thiếu máu, tăng miễn dịch.
Chỉ định điều trị phẫu thuật: Phẫu thuật điều trị UTG được chỉ định trong những trường hợp sau:
– U gan đơn độc hoặc nhiều u nhưng khu trú.
– Kích thước: Không hạn chế.
– Chưa xâm lấn các mạch máu lớn như tĩnh mạch chủ, thân tĩnh mạch cửa.
– Chưa có biểu hiện di căn xa: Cơ hoành, phổi, não.
– Nhu mô gan còn lại lành hoặc xơ nhẹ.
Đối với trường hợp cắt gan lớn cần thêm một số tiêu chuẩn:
– Chức năng gan tốt: Child A, ICG test 15’ < 15%.
– Thể tích gan còn lại đủ: >= 1% trọng lượng cơ thể.
– Không mắc các bệnh lý: Tim mạch, hô hấp, đái đường không ổn định, rối loạn đông máu…
Đối với các khối u gan thứ phát, chỉ định điều trị phẫu thuật cắt gan được đa số các tác giả thống nhất các điều kiện sau: thứ nhất khối u gan có thể cắt bỏ được, thứ 2: tổn thương nguyên phát có khả năng cắt bỏ triệt căn hoặc không có biểu hiện tái phát tại chỗ nếu khối u đã được cắt trước đó, thứ ba: không có tổn thương di căn, tái phát khác ngoài gan. Tổn thương gan sẽ được xử lý sau để tránh trường hợp việc cắt bỏ khối u gan không cần thiết khi không lấy được hết khối u nguyên phát.
- Các phương pháp cắt gan.
Kỹ thuật cắt gan của Tôn Thất Tùng (kỹ thuật cắt gan qua nhu mô).
Nguyên lý của ký thuật là cắt gan có kế hoạch, kiểm soát cuống mạch trong nhu mô. Có 2 động tác cầm máu là cặp toàn bộ cuống gan (nghiệm pháp Pringle) và đi vào trực tiếp cuống mạch trong gan thắt trước đặc biệt trong trường hợp cắt gan phải đi ngay vào ngách Gant để cặp cắt cuống phải, kỹ thuật này đơn giản, dễ thực hiện đặc biệt trong những trường hợp mổ cấp cứu, và điều quan trọng là nó tránh được những tai biến do những biến đổi về giải phẫu của các thành phần trong cuống gan.
Kỹ thuật cắt gan theo Lortat- Jacob (điển hình là cắt gan phải).
Khác cơ bản với kỹ thuật của Tôn Thất Tùng là kiểm soát, cặp cắt các thành phần cuống gan ở ngoài gan sau đó mới cắt gan, sau khi cắt các thành phần ngoài gan diện gan cắt sẽ đổi màu cho phép giải phóng gan không bị mất máu nhiều và không giới hạn thời gian cắt gan.
Kỹ thuật cắt gan theo Henri- Bismuth:
Kết hợp cả 2 phương pháp cắt gan của Tôn Thất Tùng và Lortat-Jacob, chỉ kiểm soát thành phần cuống gan một bên rồi cắt nhu mô gan, tức là chỉ cặp nửa cuống gan (hemi-Pringle). Do vậy kỹ thuật cắt gan theo H. Bismuth có nhiều ưu điểm và hiện đang được áp dụng rộng rãi. Kỹ thuật này sau này được Makuchi cải tiến dùng clamp mạch máu cặp ½ cuống gan mà không phải phẫu tích, động tác này rất hiệu quả và đơn giản trong cắt ½ gan.
Ngoài ra có thêm một số phương pháp: cắt gan bằng động tác treo gan của Belghiti, kỹ thuật loại bỏ hoàn toàn mạch máu của gan trước khi cắt gan áp dụng trong một số ít trường hợp u lớn, thâm nhiễm tĩnh mạch chủ dưới.
Điều trị phẫu thuật là phương pháp có hiệu quả. Các biện pháp khác như hóa chất, miễn dịch hoặc quang tuyến chỉ là hỗ trợ và tạm thời.
5.2. Ghép gan
Trường hợp ghép gan trên người đầu tiên được tiến hành bởi Thomas Starlz (1963). Ở Việt Nam, ca ghép gan đầu tiên trên người (bệnh nhân bị teo đường mật bẩm sinh) được thực hiện tại Học viện Quân y (1 – 2004). Ung thư gan nguyên phát là một trong những chỉ định cho ghép gan, nhất là khi bệnh nhân bị ung thư gan và có xơ gan mất bù, việc cắt bỏ toàn bộ gan và tiến hành ghép gan là sự lựa chọn đúng đắn. Với phương pháp ghép gan là có khả năng chữa khỏi cả 2 bệnh ung thư gan và xơ gan. Chỉ định ghép gan được đặt ra khi khối u có kích thước < 5 cm và chỉ có không quá 3 khối u, chưa có xâm lấn mạch máu. Thời gian sống thờm trên 4 năm sau ghép gan và tỷ lệ sống thêm mà không có tái phát ung thư là tới 85% và 92%. Ghép gan từ người cho sống đối với những bệnh nhân bị ung thư gan là biện pháp ngày càng được áp dụng nhiều ở các nước châu Á.
5.3. Nút động mạch gan
Nút động mạch gan là phương pháp điều trị tạm thời, có tác dụng giảm nguồn máu động mạch nuôi dưỡng tổ chức ung thư gan. Chỉ định cho các trường hợp không còn khả năng cắt gan. Tốt nhất là nút động mạch gan riêng hoặc nút toàn bộ các mạch máu đến gan. Nút động mạch gan sẽ gây hoại tử ở trung tâm khối u, sẽ làm giảm đau, u nhỏ lại, AFP giảm. Tỷ lệ sống trên 6 tháng sau nút động mạch gan là khoảng 28%.
5.4. Các phương pháp điều trị không phẫu thuật
5.4.1. Phương pháp gây tắc mạch qua chụp động mạch gan chọn lọc TACE (transarteriall chemoembolization), TOCE (transcartheter oily chemoembolization)
Phương pháp gây tắc mạch qua chụp động mạch gan chọn lọc để điều trị ung thư gan.
5.4.2. Phương pháp phá hủy u gan qua da dưới hướng dẫn của siêu âm:
– Tiêm hóa chất vào trong khối u: cồn hay hóa chất khác (acid axetic…) thường có tác dụng tốt với những khối u nhỏ đường kính < 3 cm.
– Điều trị lạnh (cryotherapy) và vi sóng (microwave). Điều trị bằng sóng tần số radio (radiofrequency), tia laser, chựm tia siêu âm hội tụ tần số cao.
5.4.3. Hoá chất
Điều trị bằng thuốc chống phân bào, chống chuyển hóa 5 – fluouracyl, vincristin (chỉ có 10 – 15% đáp ứng).
5.4.4. Miễn dịch
– BCG (tiêm vào khối u hay tiêm trong da).
– LH1 (giống globulin).
– Levamisol.
- PHÒNG BỆNH
Nên đi khám siêu âm bụng định kỳ 3-6 tháng/ lần. Sau khi siêu âm có kết quả nghi ngờ ung thư gan thì nên nhập viện để chụp CT hoặc MRI theo chỉ định của bác sĩ. Khi mắc bệnh viêm gan B, C, phải đến bác sĩ chuyên khoa điều trị triệt đễ bệnh lý này.
– Tránh dùng chung bơm kim tiêm với người nhiễm viêm gan B; tránh ăn uống cùng chung thìa, muỗng, chén, bát với những người viêm gan C.
– Ăn uống tránh các thức ăn nhiễm hóa chất, đậu mốc. Hạn chế bia, rượu, thức uống có nồng độ cồn cao.
Tài liệu tham khảo
- Josep M. Llovet (2005). Review: Updated treatment approach to hepatocellular carcinoma. J Gastroenterology. 40.
- Tôn Thất Bách (2006), Ung thư gan nguyên phát, Bệnh học ngoại dùng cho sau đại học, Nhà xuất bản Y học.
- Trần Văn Huy (2003), Nghiên cứu dấu ấn của các virus viêm gan B,C và đặc điểm lâm sàng của ung thư biểu mô tế bào gan, Luận án tiến sĩ Y học
- Okuda K, Ohtsuki T, Otaba H et al (1985). Natural history of hepatocellular carcinoma and prognosis in relation to treatment. Study of 850 patients. Cancer. 56(4).
- Đào Thành Chương (2002), Nghiên cứu đặc điểm lâm sàng, cận lâm sàng và kết quả sớm của điều trị phẫu thuật ung thư gan nguyên phát.
- Nguyễn Đại Bình (1997), Ung thư gan nguyên phát, Bài giảng ung thư học, Nhà xuất bản y học, Hà nội, tập 1.
- Trịnh Hồng Sơn, Lê Tư Hoàng, Nguyễn Quang Nghĩa, Đỗ Đức Vân (2001). Kết quả điều trị phẫu thuật ung thư gan nguyên phát tại bệnh viện Việt Đức giai đoạn 1992-1996. Yhọc thực hành số 7.
- Llovet J. M, Burroughs A, Bruix J (2003), Hepatocellular carcinoma, Lancet
- Ryder S.D (2003). Guidelines for the diagnosis and treatment of hepatocellular carcinoma (HCC) in adults. Gut. 52 (3).1111-1118
- Adrian M. Di Bisceglie (1999). Malignant Neoplasms of the Liver. Diseases of the Liver.(2).
- Phan Thị Phi Phi, Trương Mộng Trang, Trần Thị Chính và cs (1991). Tần suất HBsAg trong huyết thanh bệnh nhân ung thư gan nguyên phát ở Việt nam. Y học Việt Nam
- JangJW et al (2004). Transarterial chemo – lipiodolization can reativatehepatitis B virus replication in patients with hepatocellular carcino ma. JHepatol, 41 (3).
- Vũ Văn Vũ và cộng sự (2009). Điều trị dự phòng hoạt hóa viêm gan siêu virus B bằng Lamivudine trước hóa trị ung thư. Y học TP.HCM chuyên đề ung bướu học. 13 (6).
- CollierJD, Curless R, Bassendine MF, et al (1994). Clinical features andprognosis of hepatocellular carcinoma in Britain in relation to AgeAgeing.
- Nguyễn Khánh Trạch (2003). Ung thư gan nguyên phát. Bài giảng bệnh học nội khoa Tập 2.
- Trần Văn Hợp (2006), Giải phẫu bệnh học của ung thư gan nguyên phát, Ung thư gan nguyên phát, Nhà xuất bản Y học.
- ChevretS, Trinchet JC, Mathieu D, et al (1999). A new prognosticclassification for predicting survival in patients with J Hepatol; 31.
- Venk Bhat, Mamatha Bhat, Hepatic Fibrosis: Novel strategies in detection & therapy, MJM, 2008
- Na gao T, Kondo F, Sato T, Nagato Y, Kondo Y (1995). Immunohistochemical detection of berran 53 pression inhepatocellular carcinoma: correlation with cell proliferative activity indices,including mitotic index and MIB 1 immunostaining.Hum Pathol,
- Nzeako UC, Goodman ZD, Ishak KG (1996) Hepatocellular carcinoma in cirrhotic and noncirrhotic livers. A clinico-histopathologic study of 804 North American patients. Am J Clin Pathol 105.