I. Đại Cương
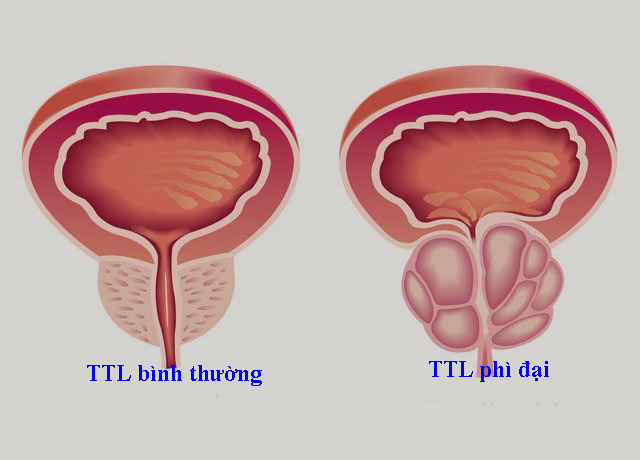
U phì đại lành tính tuyến tiền liệt là sự phát triển lành tính của tuyến tiền liệt, gây ra những biến loạn cơ năng và thực thể ở vùng cổ bàng quang, đặc biệt là làm cản trở dòng tiểu đi ra từ bàng quang.
• Tần số xuất hiện u phì đại TLT tăng lên theo tuổi, nhưng không có sự liên quan tới chế độ ăn, chủng tộc và thành phần xã hội. Trên thế giới ước tính có khoảng 30 triệu người mắc chứng bệnh phì đại tuyến tiền liệt.
• Thường xuất hiện ở đàn ông > 45 tuổi.
• Theo Berry ở độ tuổi 40-50, 20% mắc u phì đại TLT 51-60, 50%
• Ở độ tuổi 70, >70% đàn ông mắc u phì đại TLT.
• Ở độ tuổi 80, 75%.
II. Nguyên Nhân:
Hiện nay nguyên nhân của bệnh chưa được rõ. Tuy nhiên, hai yếu tố quan trọng của bệnh sinh u phì đại lành tính TLT là: tuổi già và tinh hoàn còn chức năng. Ở tuổi bắt đầu cao sự kiểm soát nội tiết thay đổi. Testosteron toàn phần và tự do giảm, estrogene tăng như có tác động gián tiếp thụ cảm testosteron dihydrotestosteron (DHT) gây phì đại TLT.
DHT có ái lực mạnh gấp năm lần testosterone với tế bào TLT. Nghiên cứu thấy rằng nồng độ 5 anpha reductase tăng cao trong tổ chức đệm của bn mắc phì đại TLT. Điều này khẳng định vai trò của DHT trong bệnh sinh phì đại TLT và tác dụng của finesteride phong tỏa enzym 5 anpha reductase trong điều trị u phì đại TLT.
Tỷ lệ u phì đại TLT ở người 40 tuổi là 8%, ở người 90 tuổi là 90%. Một khi u xuất hiện thì nó liên tục phát triển. Người ta ước tính u TLT tăng trung bình 20g trong 10 năm. Vai trò của tinh hoàn:
Huggins 1941 nhận thấy những con chó cắt tinh hoàn không bị phì đại TLT, đã áp dụng cắt tinh hoàn để điều trị u phì đại TLT (ít hiệu quả).
Gloyna, Garnet 1989 tiêm dihydrotestosteron cho chó thực nghiệm còn tinh hoàn gây phì đại TLT.
Sinh lý bệnh:
Sự tăng sinh TTL gây kích thích các thụ cảm vùng cổ bàng quang, vỏ bao TLT gây co thắt cơ trơn tạo ra hội chứng bế tắc đường tiết niệu dưới.
Khối lượng U phì đại TLT và các mô xơ phát triển nhiều cũng gây nên rối loạn bế tắc đường tiểu.
Đáp ứng của cơ bàng quang. Khi có tắc nghẽn dòng tiểu, cơ BQ tăng co bóp, dần phì đại bởi các sợi collagen càng dễ bị kích thích không ổn định, đồng thời cũng giảm đi việc đáp ứng các phản xạ bình thường gây tiểu rắt,tiểu vội, tiểu đêm. Cùng với sự tắc nghẽn kéo dài bàng quang giãn to dần, có chỗ yếu thành túi thừa, ứ đọng hay trào ngược BQ-NQ thận: nhiễm khuẩn và suy thận. Khoảng 10% bn phì đại TLT có suy thận ớ các mức độ khác nhau.
III. Giải phẫu :
Về mặt đại thể u phì đại có dạng tròn đều gồm hai thùy bên nằm ở hai bên niệu đạo, đôi khi có thuỳ thứ ba ở phía sau thường nằm sâu về phía bàng quang và gây cản trở cổ bàng quang đó là thuỳ giữa, các thuỳ này được bọc trong một lớp vỏ – gọi là vỏ TLT.
Ở người 30 tuổi, trọng lượng TLT trung bình là 20g. Trọng lượng TLT trung bình ở nhóm bệnh nhân phì đại TLT là 33g, trọng lượng u lớn nhất công bố trong y văn là 820g. 4% bn u phì đại TLT có trọng lượng trên 100g.
Trọng lượng u phì đại thể có thể thay đổi từ 10-300gr.
Năm 1988 Mc Neal sử dụng danh từ vùng trung tâm và ngoại vi tiền liệt tuyến và vùng chuyển tiếp nối giữa hai vùng này.
Theo Mc Neal; TLT được chia thành 5 vùng:
1. Vùng ngoại vi – tương ứng với vùng đuôi theo phân chia của Gil-vernet. Là phần lớn nhất, chiếm khoảng 70%, nằm ở phía sau và hai bên niệu đạo. Là phần hay phát sinh ung thư TLT.
2. Vùng trung tâm, nhỏ hơn, nằm phía sau niệu đạo, là vùng có ống dẫn tinh đi qua tới ụ núi.
3. Vùng chuyển tiếp, nhỏ nhất chiếm 5% khối lượng TLT ở người 30 tuổi, nằm hai bên niệu đạo, nó phát triển theo tuổi, phụ thuộc hormon nam. Đây là vùng gây tăng sinh u phì đại tiền liệt tuyến và tạo thành hai thùy bên TLT.
4. Vùng tuyến xung quanh niệu đạo, nó phát triển như một tay áo theo chiều dài niệu đạo TLT. Đây cũng là nơi phát triển tạo nên thùy giữa TLT.
5. Vùng xơ cơ phía trước, tương ứng với các sợi cơ thắt vân ở phía trước TLT.
Lợi ích của việc phân chia này là thấy được rõ trên siêu âm. Phì đại TLT thường phát triển ở vùng chuyển tiếp
IV. Chẩn Đoán
4.1. Lâm sàng
4.1.1. Triệu chứng cơ năng
Đó là biểu hiện sớm hay muộn của loại hội chứng đường tiết niệu thấp do vị trí khối u, viêm nhiễm hay rối loạn thần kinh cổ bàng quang. Khái niệm “Hội chứng đường tiết niệu thấp” được đưa ra to năn 1994 và tái khẳng định vào năm 2002.
Các triệu chứng do kích thích :
• Đái nhiều lần nhất là về ban đêm gây mất ngủ.
• Đái vội: đột nhiên Bn có cảm giác buồn đái dữ dội, có cảm giác nước tiểu són ra ngoài không kiểm soát được.
• Đái buốt thường kết hợp với viêm đường tiết niệu.
Các triệu chứng do chèn ép : (H/c, tắc nghẽn) bệnh nhân đái khó, phải rặn, tia nước tiểu yếu, đái xong không có cảm giác thoải mái.
Có khi bệnh nhân biểu hiện các triệu chứng :
• Bí đái hoàn toàn. 25% bn u phì đại TLT đến khám vì bí đái cấp tính.
• Nhiễm khuẩn tiết niệu (viêm bàng quang, TLT mào tinh hoàn).
4.2. Thăm khám lâm sàng
Đánh giá mức độ đái khó qua thang điểm IPSS (the International Prostate Symptom Score) chia thành ba mức độ :
• Nhẹ : 0- 7 điểm
• Trung bình : 8-20 điểm
• Nặng : 21-35 điểm
• Khám thận, vùng hạ vị cầu bàng quang và tinh hoàn 2 bên. Dương vật bao quy đầu.
Thăm trực tràng :
• Là động tác khám cơ bản.
• Bệnh nhân nằm ngửa, đưa ngón trỏ thăm trực tràng phối hợp với tay ở vùng hạ vị. Phát hiện ở thành trước trực tràng ngay sau xương mu, một khối tròn đều, nhẵn, đàn hồi, đồng nhất, không đau. Cần thăm khám bề mặt cũng như chu vi tuyến để ước lượng kích thước.
• Đôi khi thấy tuyến không đều có nhân cứng hoặc gắn chặt vào xương mu đó là biểu hiện của ung thư tiền liệt tuyến. Phát hiện 14-30% trường hợp K TLT khi PSA bình thường.
• Phát hiện các bệnh lý hậu môn trực tràng: trương lực cơ thắt, u trực tràng…
4.3. Các khám nghiệm cận lâm sàng
4.3.1. Siêu âm
Có thể thực hiện theo đường trên xương mu hoặc qua trực tràng.
Thấy khối TLT đồng nhất thường có hai thuỳ đối xứng nhau qua đường giữa. Cho phép ước lượng trọng lượng của u qua công thức :
L x H x W
V = ————————-
2
Cho phép thăm dò hai thận, bàng quang và đo lượng nước tiểu cặn trong bàng quang.
Có thể thấy các ổ rỗng âm, các thùy tuyến tiền liệt không đồng nhất là những dấu hiệu nghi nghờ K TTL.
4.3.2. Kháng nguyên đặc hiệu TLT (PSA)
Nó đặc hiệu cho TLT, tuy nhiên có giá trị trong việc chẩn đoán ung thư TLT vì khi ung thư PSA thường tăng cao.
Bình thường <4ng/ml.
PSA>10ng/ml 50% nguy cơ ung thư cần làm sinh thiết TLT.
PSA 4-10 ng/ml là khoảng ghi ghờ cần lưu ý theo dõi.
• PSA từ 4-10ng/ml: tỷ lệ UT là 18-25% (trung bình là 21%)
• PSA > 10ng/ml: tỷ lệ UT khoảng 58%-80% (trung bình là 60%).
• PSA > 20ng/ml: tỷ lệ UT khoảng 90%.
Chụp niệu đồ tĩnh mạch ít có giá trị đối với u phì đại TLT.
Soi bàng quang, niệu đạo: giúp chẩn đoán phân biệt các nguyên nhân đái máu do TLT hay do u bàng quang. Xác định nguyên nhân đái khó do cổ bàng quang, TLT, hoặc do hẹp niệu đạo.
4.3.3. Các XN khác
Động học nước tiểu, đánh giá áp lực bàng quang, niệu đạo và lưu lượng nước tiểu.
Xác định thời gian một lần tiểu (15-17 giây). Khối lượng một lần tiểu (250-350ml)
Lưu lượng dòng tiểu Qmax 19,6 ml/gy. Khi Qmax>15ml/gy coi như chưa có bế tắc đường tiết niệu, Qmax10-15ml/gy: theo dõi. Qmax<10ml/gy tắc nghẽn niệu đạo hoặc cơ bàng quang yếu.
Đo lượng nước tiểu tồn đọng bằng cách: siêu âm hoặc đặt thông tiểu sau khi Bn tiểu tiện. R>200 ml ứ đọng nước tiểu có ý nghĩa bệnh lý của BPH.
• XN sinh hoá : US, Creatircine máu.
• Cấy vi khuẩn nước tiểu.
4.4. Chẩn đoán xác định:
Dựa vào triệu chứng lâm sàng và cận lâm sàng đã nêu trên.
4.5. Chẩn đoán phân biệt
4.5.1. Ung thư tiền liệt tuyến :
Bệnh cũng hay gặp ở người cao tuổi nên cần chú ý để tránh nhầm với K TLT, dựa vào :
– Khám trực tràng : TLT rắn or có nhân rắn ranh giới không đều.
– Siêu âm : Tiền liệt tuyến không đồng nhất, có ổ rỗng âm, các thuỳ không đối xứng nhau.
– PSA tăng cao trong ung thư TLT > 10mg/ml.
– Nếu nghi ngờ cần sinh thiết để khẳng định chẩn đoán.
4.5.2. Phân biệt với các nguyên nhân đái khó khác như
Xơ cứng cổ bàng quang
• Lâm sàng bệnh nhân cao tuổi (trên 60 tuổi)
• Đái khó, có khi bí đái phải đặt ống thông niệu đạo.
• Thăm trực tràng TTL không to
• Siêu âm: không phát hiện phì đại tuyến tiền liệt
• PSA bình thường
• Niệu động học xác định đái khó do tắc nghẽn cổ bàng quang
• Soi bàng quang niệu đạo: hình ảnh xơ chít cổ bàng quang
Bàng quang thần kinh
• Bệnh nhân có tiền sử chấn thương cột sống, tai biến mạch não
• Đái khó kèm rỉ nước tiểu
• Khám lâm sàng thấy cầu bàng quang căng to
• Thăm trực tràng tuyến tiền liệt không to
• Siêu âm TTL không to, bàng quang giãn ứ nước tiểu, có khi giản cả hai niệu quản.
• PSA máu bình thường
• Động học nước tiểu: không thấy tín hiệu co bóp của cơ bàng quang.
Hẹp niệu đạo
• Bệnh nhân có tiền sử chấn thương chấn thương niệu đạo hoặc can thiệp quan đường niệu đạo.
• Đến khám vì đái khó hoặc bí đái
• Khám có cầu bàng quang, thăm trực tràng tiền liệt tuyến không to. Có khi có chít hẹp lỗ ngoài niệu đạo do viêm nhiễm chí hẹp bao qui đầu.
• Siêu âm TTL không to, bàng quang giãn ứ nước tiểu, có khi giản cả hai niệu quản.
• PSA máu bình thường
• Động học nước tiểu: hình ảnh tắc nghẽn niệu đạo
• Chụp bàng quang niệu đạo ngược dòng: hình ảnh hẹp niệu đạo
Viêm hoặc áp xe tiền liệt tuyến
• Ít gặp ở người già, thường gặp ở lứa tuổi trung niên.
V. Điều trị
Nguyên tắc điều trị chỉ định điều trị dựa vào mức độ nghiêm trọng của các triệu chứng, mức độ bận tâm và nguyện vọng của bệnh nhân. Thông tin về nguy cơ và lợi ích của việc lựa chọn điều trị BPH nên được giải thích cho tất cả các bệnh nhân.
5.1. Phương pháp điều trị bằng thay đổi cách sinh hoạt và theo dõi,chờ đợi
– Chỉ định: Bệnh nhân có triệu chứng nhẹ (ví dụ, IPSS <7) nên được tư vấn về một sự kết hợp sửa đổi cách sinh hoạt cho phù hợp với cách điều trị là theo dõi và chờ đợi.
– Điều trị cụ thể:
Bệnh nhân được theo dõi và thăm khám bác sỹ theo dõi định kỳ. Tùy chọn: Bác sĩ ghi nhận tình trạng bệnh lúc ban đầu, mức độ nghiêm trọng của hội chứng kích thích, tuyến tiền liệt khối lượng và / hoặc PSA huyết thanh để tư vấn cho bệnh nhân nguy cơ tiến triển triệu chứng bí tiểu cấp tính hoặc trong tương lai cần phẫu thuật liên quan đến BPH (những yếu tố nguy cơ xác định các bệnh nhân có nguy cơ cho sự tiến triển). Một loạt các thay đổi lối sống có thể được đề nghị cho bệnh nhân có triệu chứng.
• Hạn chế uống nước trước khi đi ngủ
• Tránh thức uống chứa caffeine, thức ăn cay
• Tránh sử dụng một số loại thuốc (ví dụ, thuốc lợi tiểu, thuốc thông mũi, thuốc kháng histamin, thuốc chống trầm cảm)
• Luyện tập cách tiểu tiện giúp bàng quang hoạt động tốt.
• Bài tập tăng sức mạnh sàn chậu
• Tránh hoặc điều trị táo bón
5.2. Điều trị nội khoa
Chỉ định:
• Điều trị tùy chọn cho bệnh nhân khó chịu vừa phải (ví dụ như, IPSS 8 – 18).
• Chỉ định đối với giai đoạn 1 và 2 của bệnh nghĩa là u chưa gây cản trở nhiều tới hệ tiết niệu. Lượng nước tiểu tồn dư trong bàng quang < 100ml.
• Có tác dụng chống co thắt và phù nề vùng cổ bàng quang TLT.
Thuốc đối kháng alpha – Adrenergic:
• Có tác dụng làm giãn cơ trơn nhờ tác động trên các thụ thể anpha – adrenergic ở vùng cổ bàng quang và TLT. Các thuốc này có thể làm hạ huyết áp.
• Doxazosin (cardural) ức chế alpha – adrenergic sau sinape, liều 2mg/24h.
• Tamsulosin ( Flomax) ức chế đặc hiệu alpha 1 receptors, liều 0,4-0,8 mg/24h.
• Alpha-blockers là lựa chọn diều trị đầu tiên cho người đàn ông có triệu chứng đường tiết niệu dưới do PBH, những người mong muốn điều trị. Alfuzosin, doxazosin, tamsulosin và terazosin là những thuốc được lựa chọn điều trị thích hợp cho LUTs thứ cấp. Tuy nhiên, chúng không làm thay đổi sự tiến triển tự nhiên của bệnh. Mặc dù có sự khác biệt trong thành phần hóa học của các thuốc này, tất cả 4 loại thuốc này đều có hiệu quả lâm sàng như nhau. Sự lựa chọn của loại thuốc nào nên tùy thuộc vào các bệnh đi kèm của bệnh nhân, tác dụng phụ và khả năng dung nạp thuốc của bệnh nhân.
Thuốc tác động vào sự chuyển hoá của androgen với ý định ngăn cản sự phát triển của u phì đại TLT.
Finasteride (Proscar) ức chế chuyển hoá testosterone thành dihydrotestosterone (DHT), liều 5mg/24h.
Thuốc ức chế 5 alpha-reductase (dutasteride và finasteride) là phương pháp điều trị thích hợp và hiệu quả cho bệnh nhân kết hợp với tác động hạn chế sự phát triển của tuyến tiền liệt. Một số nghiên cứu đã chứng minh rằng, ngoài các triệu chứng cải thiện, tiến triển tự nhiên của BPH có thể được thay đổi thông qua việc giảm nguy cơ bí tiểu cấp tính (AUR) và sự cần thiết phải can thiệp phẫu thuật.
Các thuốc thảo mộc có tính chất chống viêm chống phù nề.
Nghiên cứu của Madersbacher và cộng sự năm 2004 và Roehborn năm 2008 cho thấy rằng; điều trị bằng đối kháng anpha-adrenergic có tác dụng cải thiện cải thiện triệu chứng và dòng tiểu, tác dụng này rõ rệt sai 1-2 tuần điều trị. Tuy nhiên điều trị bằng Finasteride còn có tác dụng giảm khối lượng u và giảm nguy cơ bí tiểu cấp và phẫu thuật. Nghiên cứu của Mc Connell và cộng sự 2003 cho thấy phối hợp điều trị cho tác dụng tốt hơn đơn trị liệu. Tuy nhiên tác dụng này rõ rệt sau 1 năm điều trị.
Điều trị kết hợp (alpha-blocker và chất ức chế 5 alpha-reductase)
Sự kết hợp thuốc alpha-adrenergic và thuốc chất ức chế 5 alpha-reductase là một chiến lược điều trị thích hợp và hiệu quả cho bệnh nhân kết hợp điều trị giảm sự phát triển tuyến tiền liệt. Kết quả thử nghiệm lâm sàng đã chỉ ra rằng điều trị kết hợp cải thiện đáng kể trong điểm số triệu chứng và lưu lượng nước tiểu so với đơn trị liệu. Bệnh nhân điều trị thành công có thể ngưng điều trị alpha-blocker sau 6 đến 9 điều trị tháng. Nếu các triệu chứng tái phát, alpha-blocker được khởi động lại.
5.3. Điều trị ngoại khoa
5.3.1. Chỉ định
Việc chỉ định các phương pháp điều trị tuỳ thuộc vào kích thước của u. Chỉ định điều trị ngoại khoa trong các trường hợp :
• U gây ảnh hưởng nhiều đến đường tiết niệu, lượng tiểu cặn > 100ml, đái khó nhiều Qmax < 10ml/s.
• Bí đái cấp phải đặt sonde niệu đạo.
• Nhiễm khuẩn niệu, sỏi bàng quang, túi thừa BQ.
• Đái máu mức độ nặng, suy thận (khoảng 10% bệnh nhân phì đại TLT có dấu hiệu suy thận).
5.3.2. Phương pháp cắt nội soi qua niệu đạo
Được coi là phương pháp chuẩn vàng trong điều trị phẫu thuật HBP.
Mục đích của phẫu thuật cắt bỏ tuyến tiền liệt trong điều trị phì đại lành tính tuyến này (BPH) là nhằm lấy đi khối mô gây hẹp niệu đạo, trong khi chỉ làm tổn hại tối thiểu tới các cấu trúc ở xung quanh.
Hãy cố gắng cắt tất cả khối mô của tuyến tiền liệt có thể cắt được, mà không làm thủng bao tuyến, hoặc kéo dài thời gian mổ một cách không cần thiết. Thật vậy, phần mô tuyến còn sót có thể tăng trưởng lại, tạo điều kiện cho nhiễm khuẩn, làm tăng hấp thu dịch tưới-rửa (fluid absorption), và có xu hướng chảy máu. Một châm ngôn (axion) của ngành tiết niệu cổ đã khẳng định “Không phải là cắt bỏ đi bao nhiêu, mà là để lại bao nhiêu thì sẽ gây ra các vấn đề hậu-phẫu”
Phẫu thuật cắt bỏ tuyến tiền liệt qua đường niệu đạo (TURP) là một biện pháp có thách thức đáng ngạc nhiên, và đòi hỏi một thời gian huấn luyện kéo dài. Các bệnh nhân nam giới, đã cao tuổi, và kém khỏe mạnh là các đối tượng có xu hướng yêu cầu được điều trị bằng biện pháp phẫu thuật này. Cũng nên ghi nhận rằng, các cải tiến liên tục về trang thiết bị dụng cụ và kỹ thuật đã cho phép các phẫu thuật viên thực hiện phẫu thuật này dễ dàng hơn, và các bệnh nhân ít bị nguy hiểm hơn.
Chỉ định đối với những u nhỏ và vừa trọng lượng < 70g.
Chỉ định tương đối để lựa chọn giữa cắt bỏ tuyến tiền liệt bằng phẫu thuật mở và phẫu thuật cắt bỏ tuyến tiền liệt qua đường niệu đạo (TURP) thường dựa trên hai căn cứ là: thể tích của tuyến, và khả năng của phẫu thuật viên liệu có hoàn thành được phẫu thuật qua đường niệu đạo (TURP) với một thời gian mổ thật sự chỉ trong vòng 90 phút hay không (mặc dù thời gian này được coi là tối ưu nếu < 60 phút).
Các chống chỉ định:
Một số chống chỉ định tương đối là: tình trạng tim-phổi không ổn định (unstable cardopulmonary status) và có bệnh sử rối loạn chảy máu (bleeding disorders) không thể sửa chữa. Các bệnh nhân mới bị nhồi máu cơ tim hoặc được đặt stent động mạch vành tim đều không được chỉ định phẫu thuật cắt bỏ tuyến tiền liệt qua đường niệu đạo (TURP) trong vòng ít nhất 1 tháng , bởi vì phẫu thuật này có thể làm tăng nguy cơ xảy ra thêm các tai biến tim-mạch hoặc các biến chứng khác. Đã có ý kiến cho rằng, nên trì hoãn một thời kỳ tối thiểu 3 tháng là hợp lý; nhưng, sau bất kỳ sự kiện cơ tim đáng kể nào thì, đợi đến 6 tháng sau mới thực hiện phẫu thuật cắt bỏ tuyến tiền liệt (TURP) lại là giải pháp tối ưu.
Các bệnh nhân bị bệnh nhược cơ nặng (myasthenia gravis), bệnh xơ cứng rải rác hoặc đa xơ cứng (multiple sclerosis), hoặc bệnh Parkinson với rối loạn chức năng cơ thắt ngoài niệu đạo, và/hoặc tăng trương lực bàng quang (hypertonic bladder) nặng thì, đều không được phẫu thuật cắt bỏ tuyến tiền liệt qua đường niệu đạo (TURP), bởi vì trong các hoàn cảnh nói trên thì phẫu thuật này chắc chắn sẽ dẫn tới tình trạng tiểu tiện mất chủ động khó chữa.
Các bệnh nhân đã từng bị gãy xương chậu mà có kèm thương tổn ở cơ thắt ngoài niệu đạo thì, cũng không được phẫu thuật cắt bỏ tuyến tiền liệt theo đường niệu đạo (TURP) vì cùng một lý do như trên. Phẫu thuật cắt bỏ tuyến tiền liệt theo đường niệu đạo (TURP), có thể làm mất cơ thắt trong niệu đạo, nên sẽ đảy các bệnh nhân kể trên lâm vào tình trạng lệ thuộc hoàn toàn vào hoạt động của cơ thắt ngoài niệu đạo thì mới có thể vẫn duy trì được tiểu tiện chủ động. Nếu cơ thắt ngoài niệu đạo lại bị tổn hại, hoặc thương tổn, hoặc rối loạn chức năng nữa thì, sẽ phát sinh vấn đề tiểu tiện mất chủ động.
Nhiễm khuẩn đường tiết niệu đang diễn biến cũng là một chống chỉ định khác của phẫu thuật cắt bỏ tuyến tiền liệt qua đường niệu đạo (TURP). Thông thường, có thể phải xếp lịch lại để phẫu thuật, tùy theo diễn biến của nhiễm khuẩn trong quá trình bệnh nhân được điều trị bằng các thuốc kháng sinh thích hợp.
Ưu điểm :
Là phương pháp ít gây sang chấn, ngày càng được áp dụng rộng rãi (80-90%
số bệnh nhân được điều trị bằng phương pháp này ở các nước tiên tiến).
• Thời gian nằm viện ngắn.
• Hiệu quả tốt về mặt tiểu tiện.
• Hiện nay được coi là phương pháp chuẩn trong điều trị u phì đại lành tính TTL.
Tỷ lệ tái phát sau mổ nội soi là 18%, tỷ lệ tử vong 0.23%.
Cho tới hiện nay chưa có một liệu pháp nội khoa nào, hoặc một biện pháp phẫu thuật thay thế hiện hữu nào, lại có thể mang lại mức cải thiện tổng thể dài-hạn về mặt tốc độ dòng tiểu tiện, và về số điểm theo thang đánh giá triệu chứng, cho tất cả các bệnh nhân phì đại tuyến tiền liệt lành tính (BPH) có triệu chứng, ngang với mức độ cải thiện mà phẫu thuật cắt bỏ tuyến tiền liệt qua đường niệu đạo (TURP) mang lại.
Nguy cơ biến chứng của phẫu thuật thường liên quan với những u có kích thước lớn > 45g, thời gian phẫu thuật kéo dài > 90 phút.
Hội chứng TURP
Nếu được hấp thu vào cơ thể với một lượng lớn, glycine có thể ức chế dẫn truyền sung thần kinh, và có thể gây rối loạn thị giác, tuy hai tác dụng phụ này hiếm xảy ra. Trong các trường hợp glycine được hấp thụ vào cơ thể với một lượng nhiều hơn 1.000 mL thì, đã xảy ra các triệu chứng sau đây: cảm giác bị kim châm (prickling sensations), tăng buồn nôn, hạ huyết áp, nhịp tim chậm, và lú lẫn (confusion). Khi lượng glycine được hấp thụ vào cơ thể càng nhiều hơn thì, các hiệu quả không mong muốn mà nó gây ra càng tăng dần. Các hiệu quả không mong muốn này trở nên nghiêm trọng, khi lượng glycine được hấp thụ là 3.000 mL hoặc nhiều hơn. Trong một phẫu thuật cắt bỏ tuyến tiền liệt qua đường niệu đạo, trung bình mỗi phút có gần 20 mL dịch được hấp thụ vào trong cơ thể, hoặc ngay trong giờ đầu tiên của cuộc mổ thì, đã có gần 1.000-1.200 mL dịch được hấp thu. Một phần ba lượng dịch này được hấp thu trực tiếp vào trong hệ thống tĩnh mạch.
Hiện tượng này có thể dẫn tới tình trạng giảm-natri huyết do loãng máu (tức là hội chứng TUR), biểu hiện lâm sàng bởi các triệu chứng: tinh thần lú lẫn (mental confusion), buồn nôn, nôn, rối loạn thị giác (visual disturbances), tan huyết, bệnh thận hemoglobin (hemoglobin nephropathy), hôn mê, và sốc. Về mặt huyết động học, lúc khởi đầu, hội chứng này đặc trưng bởi tăng huyết áp tĩnh mạch trung tâm, tăng huyết áp động mạch, nhịp tim chậm, và các dấu hiệu khác, vốn là các biểu hiện của tình trạng quá tải ở hệ mạch máu (vascular overload), bao gồm: bồn chồn không yên (restlessness), nhịp tim nhanh, và đôi khi da, kết mạc mắt, các niêm mạc, hoặc móng tay đổi màu thành nhợt nhạt (dusky changes). Các triệu chứng của hội chứng cắt qua dường niệu đạo (TUR syndrome), nói chung, chỉ xuất hiện khi mức natri trong huyết thanh giảm xuống tới mức 125 mEq, hoặc thấp hơn nữa.
Theo ước lượng thì có khoảng 2% số bệnh nhân trải nghiệm hội chứng cắt qua đường niệu đạo (TUR syndrome) ở các mức độ khác nhau. Nguy cơ xảy ra hội chứng cắt qua đường niệu đạo (TUR syndrome) tăng lên ở các bệnh nhân với tuyến tiền liệt phì đại to hơn 45 gam, hoặc khi thời gian mổ kéo dài quá 90 phút, và khi bệnh nhân ngay từ trước phẫu thuật đã bị giảm-natri huyết tương đối. Do đó, chỉ nên đề nghị phẫu thuật cắt bỏ tuyến tiền liệt qua đường niệu đạo (TURP), khi phẫu thuật viên, sẽ đảm nhiệm cuộc mổ, tin tưởng một cách hợp lý rằng, mình sẽ có khả năng kết thúc phẫu thuật này trong vòng không quá 90 phút.
Nguy cơ bị hội chứng cắt qua đường niệu đạo (TUR) sẽ giảm bớt, nếu sử dụng dung dịch không gây tan huyết để tưới rửa trong lúc tiến hành phẫu thuật, và duy trì dòng đi vào của dịch tưới rửa ở mức áp suất càng thấp càng tốt. Một nghiên cứu của Madsen và Naber đã thấy rằng, lượng dịch được hấp thụ vào cơ thể tỷ lệ thuận với áp suất dịch tưới rửa (irrigation fluid pressure). Chỉ cần nâng độ cao của bình đựng dung dịch tưới rửa từ 60 cm lên 70 cm, cũng đã làm tăng gấp đôi áp suất tưới rửa. Các tác giả này cũng thấy rằng, để giữ cho phẫu thuật viên luôn luôn nhìn rõ phẫu trường thì, tốc độ tưới rửa (irrigation rate) cần phải có là 300 mL/phút, và tốc độ này không thể được duy trì thích đáng, nếu bình đựng dung dịch tưới rửa chỉ được treo ở độ cao thấp hơn 60 cm. Hệ thống tưới rửa liên tục có xu hướng giữ áp suất trong bàng quang luôn thấp, và giúp làm giảm thiểu lượng dịch được hấp thụ vào cơ thể. Nếu không sử dụng phương pháp tưới rửa liên tục thì, để giảm thiểu hấp thu dịch, phẫu thuật viên thường xuyên phải tháo rỗng bàng quang, trước khi bàng quang đày tới mức tối đa, hoặc mỗi khi phẫu thuật viên không nhìn được rõ ràng qua ống soi-cắt.
Trong trường hợp xảy ra giảm-natri huyết nhẹ hoặc trung bình thì, điều trị cho bệnh nhân bằng cách truyền tĩnh mạch dung dịch nước muối đẳng trương và furosemide (Lasix) cũng có thể là đủ. Biện pháp điều trị này làm giảm quá tải dịch (fluid overload), thông qua hiệu quả lợi niệu của furosemide, đồng thời vẫn duy trì được nồng độ của natri trong huyết thanh. Phải khởi động điều trị với furosemide, ngay từ khi bệnh nhân vẫn còn ở trong phòng mổ, nếu gặp các hoàn cảnh sau đây: có hiện tượng chảy máu không bình thường, thời gian mổ kéo dài nhiều hơn 90 phút, hoặc nếu mức natri trong huyết thanh của bệnh nhân hạ thấp nhanh chóng.
Trong các trường hợp giảm-natri huyết nặng thì, tốt nhất là điều trị bằng truyền tĩnh mạch chậm dung dịch nước muối ưu trương 3%, thông thường từ 150 đến 200 mL, với tốc độ truyền trong khoảng từ 1 đến 2 giờ. Biện pháp điều trị này bao giờ cũng phải đi kèm với liệu pháp lợi niệu (furosemide theo đường tĩnh mạch), đặc biệt là ở các bệnh nhân có nguy cơ cao bị suy tim sung huyết (CHF: congestive heart failure). Có thể nhắc lại liệu pháp dung dịch nước muối ưu trương nếu thấy cần thiết. Tuy nhiên, trong khi bệnh nhân đang được truyền dung dịch nước muối ưu trương 3% thì, cứ từng 2-4 giờ một lần, phải theo rõi cẩn thận các chất điện giải (electrolytes), nhằm phòng ngừa sửa chữa quá mức các sai lệch.
Các bệnh nhân bị giảm-natri huyết mà có triệu chứng thì, nói chung, có thể làm mất triệu chứng, bằng cách bổ sung natri huyết thanh tới đúng mức 4-6 mEq/L. Điển hình là, trong vòng 12-24 giờ đầu tiên nếu thực trạng thiếu hụt natri không nhiều hơn một nửa của mức thiếu hụt theo dự kiến thì không cần sửa chữa, và để đảo ngược tình trạng thiếu hụt này bằng truyền dung dịch nước muối ưu trương 3% thì cũng không nhiều hơn một nửa lượng natri bị thiếu hụt. Hãy chuyển từ nước muối ưu trương 3% sang nước muối đẳng trương càng sớm càng tốt. Hãy điều chỉnh tốc độ truyền nước muối bổ sung, sao cho lượng natri tuyệt đối trong huyết thanh không tăng lên cao hơn mức 20 mEq/L trong một khoảng thời gian 24 giờ. Thường thì dung dịch nước muối được yêu cầu truyền với tốc độ chậm.
Vì dung dịch nước muối ưu trương 3%, nói chung, được sử dụng để bổ sung không nhiều hơn một nửa tổng lượng muối cần phải được thay thế, nên tổng thể tích không quá 300-500 mL dung dịch nước muối ưu trương 3% là liều lượng hợp lý, ở hầu hết các bệnh nhân, thậm chí ở các bệnh nhân bị giảm-natri huyết nặng. Một khi đã rõ ràng không còn bất kỳ các triệu chứng của giảm-natri huyết nào nữa, và mức natri trong huyết thanh của bệnh nhân đã được cải thiện thì, thay vì dung dịch nước muối ưu trương 3% chuyển sang tiếp tục truyền dung dịch nước muối đẳng trương.
Có thể ước lượng lượng natri thiếu hụt theo công thức sau đây: Ước lượng natri thiếu hụt = (140 − natri đang có trong huyết thanh)(trọng lượng cơ thể bằng kilogam)(0,6) . Ví dụ, một bệnh nhân nặng 70 kg, với mức natri trong huyết thanh đang là 120, sẽ có ước lượng thiếu hụt natri là 840 mEq. Thể tích dung dịch nước muối dùng để bổ sung, nhằm đưa mức natri huyết thanh trở lại hoàn toàn bình thường, có thể được tính toán dễ dàng bằng cách lấy ước lượng tổng natri thiếu hụt chia cho lượng natri trong (một đơn vị-ND) dung dịch nước muối dùng để thay thế bổ sung. (Dung dịch nước muối đẳng trương chứa 154 mEq/L natri, và dung dịch nước muối ưu trương 3% chứa 513 mEq/L natri). Mục đích của liệu pháp bổ sung natri là sửa chữa tình trạng giảm-natri huyết với tốc độ chậm, nhưng đày đủ, để tránh các triệu chứng của giảm-natri huyết.
Nguy cơ tái phát u sau 5 năm là 5%.
Tỷ lệ phẫu thuật u TLT bằng phương pháp nội soi ở Mỹ và các nước bắc Âu là 97%, ở Pháp và Nhật Bản là 70%.
Các biện pháp ngoại khoa thay thế phẫu thuật cắt bỏ tuyến tiền liệt qua đường niệu đạo (TURP)
Các biện pháp ngoại khoa thay thế phẫu thuật cắt bỏ tuyến tiền liệt qua dường niệu đạo (TURP) đã được thiết kế để làm giảm mất máu, giảm thời gian bệnh nhân nằm viện, và giảm hấp thu nước, trong khi vẫn lấy đi hoặc phá hủy phần mô tuyến tiền liệt gây hẹp niệu đạo. Các biện pháp này gồm có: Phẫu thuật cắt bỏ tuyền tiền liệt qua đường niệu đạo bằng bốc hơi (vaporization TURP), cắt bỏ tuyền tiền liệt qua đường niệu đạo lưỡng-cực (bipolar TURP), làm bay hơi quang-chọn lọc tuyến tiền liệt (photoselective vaporization of the prostate), và bóc nhân bằng laser holmium (holmium laser enucleation).
Điện-bốc hơi tuyến tiền liệt (electrovaporization of the prostate)
Bốc hơi tuyến tiền liệt bằng điện (hoặc làm bốc hơi tuyến tiền liệt qua đường niệu đạo [TUVP ], hoặc làm bốc hơi bằng điện , hoặc phương pháp VaporTrode ) là kỹ thuật sử dụng một điện-cực là một thanh lăn (roller) hình trụ, có các gờ lồi (ridged) hoặc hố lõm (pitted), thay vì quai dây kim loại cắt-mô như ở các ống soi-cắt (resectoscope) chuẩn. Một dòng điện có mức năng lượng rất cao, được đưa vào điện-cực là thanh lăn hình trụ, để khi điện-cực tiếp xúc với mô của tuyến tiền liệt thì, làm bốc hơi hoàn toàn mô này. Phương pháp bốc hơi bằng điện có ưu điểm là cầm máu tương đối tốt, ít gây ra chảy máu, và hấp thu dịch tưới rửa (fluid absorption) ít hơn, so với phẫu thuật cắt bỏ tuyến tiền liệt qua đường niệu đạo (TURP) chuẩn.
Các kết quả tổng thể của phương pháp bốc hơi bằng điện cũng rất giống với của phẫu thuật cắt bỏ tuyến tiền liệt qua đường niệu đạo (TURP), mặc dù khi bệnh nhân tiểu tiện thì tốc độ của dòng tiểu tiện không thật tốt, và các triệu chứng kích thích (irritative symptoms) sau-phẫu thuật được báo cáo là hay xảy ra hơn. Bốc hơi bằng điện phải được thực hiện tương đối chậm, và để có thể được điều trị bằng phương pháp này thì, kích thước của tuyến tiền liệt có xu hướng bị hạn chế, và vào lúc kết thúc của biện pháp thì lượng mô còn lại là quá ít hoặc, không còn đủ, để được gửi đi làm xét nghiệm giải phẫu bệnh. Tuy nhiên, hiện nay đã có các điện cực làm bốc hơi/cắt (vaporization/resection elctrodes) cải tiến, mới được chế tạo, có thể mang lại cơ hội để điều trị các trường hợp tuyến tiền liệt phì đại lớn hơn, và vẫn giữ lại được đủ lượng mô tuyến cần thiết để gửi đi làm xét nghiệm giải phẫu bệnh.
Phẫu thuật cắt bỏ tuyến tiền liệt qua đường niệu đạo lưỡng-cực (Bipolar TURP)
Phẫu thuật cắt bỏ tuyến tiền liệt qua đường niệu đạo lưỡng-cực (bipolar TURP) cũng là kỹ thuật cắt mô bằng điện-phẫu thuật (electrosurgical resection), nhưng năng lượng cắt mô được chuyển giao bởi dòng điện lưỡng-cực (bipolar fashion), hơn là bởi dòng điện đơn-cực (straight monpolar current?) như trong phẫu thuật cắt tuyến tiền liệt qua đường niệu đạo (TURP) truyền thống. Các dụng cụ và kỹ thuật cắt tuyến tiền liệt qua đường niệu đạo lưỡng cực (bipolar TURP) hầu như đồng nhất giữa hai kiểu phẫu thuật nội-soi này; ngoại trừ, trong kỹ thuật lưỡng-cực thì, máy phát điện là máy lưỡng-cực (bipolar electrical generator), và các ống soi-cắt (resectoscopes) cũng như các quai kim loại cắt-mô (loops) đều đã được cải tiến một cách đặc biệt. Khi đưa dòng điện cắt-mô được đưa vào các điện-cực thì, vành plasma (plasma corona) hoặc trường ion-hóa (field of ionization) sẽ hình thành giữa hai điện-cực, đồng thời cắt đứt các cầu nối (bonds) giữa các phân tử của mô, và từ đó cắt ngang mô một cách hiệu quả. Lúc khởi thủy, các quai dây kim loại cắt-mô của hệ thống lưỡng-cực được sử dụng, là hai sợi dây kim loại đặt song song với nhau, và cách nhau 2 mm; nhưng trong các mô hình (mẫu máy) hiện nay thì lại sử dụng chỉ một quai dây kim loại duy nhất, với phần nguội (electrical ground return) được thiết kế nằm ở ngay bên trong của chuôi cầm hoặc cán (shaft) của quai dây kim loại này.
Với kỹ thuật cắt mô lưỡng-cực thì, các mô ở cạnh vị trí cắt và ở sâu ít bị thương tổn hơn, so với phẫu thuật cắt bỏ tuyến tiền liệt qua đường niệu đạo đơn-cực (monopolar TURP). Ưu điểm này có được là vì, trong phương pháp lưỡng-cực (bipolar method) thì, năng lượng điện được truyền trực tiếp giữa quai dây kim loại và cán hoặc chuôi cầm (shaft) của nó nằm ngay ở trong ống soi-cắt (resectoscope), trong khi ở phương pháp đơn-cực (monopolar method) thì, năng lượng điện lại được truyền từ điện cực là quai dây kim loại tới mô tế bào ngoại vi để trở về đất (grounding pad: cực nguội). Điều này cũng giải thích tại sao, với dụng cụ cắt lưỡng-cực thì, sau đó, mô hạt (granulation tissue) lại hình thành ít hơn. Hơn nữa, với phương pháp lưỡng-cực thì, mô bị đốt cháy ít hơn (less charring tissue); như vậy, giúp phẫu thuật viên có thể nhận định được rõ rệt bao phẫu thuật (surgical capsule) và các mốc (landmarks) giải phẫu khác.
Về tổng thể, với bộ dụng cụ lưỡng-cực thì, cầm máu có thể được cải thiện chút ít, mặc dù động tác quét nhanh (rapid sweeping) quai dây kim loại với dòng điện đông-mô (coagulating current) thường kém hiệu quả hơn, so với hệ thống đơn-cực (monopolar system). Nếu sử dụng dòng điện đông-mô trong công nghệ lưỡng-cực thì, kỹ thuật thao tác cắt mô được yêu cầu là phải tạo được sức ép trực tiếp lên các vị trí chảy máu. Các mảnh nhỏ (chips) được cắt ra từ tuyến tiền liệt sẽ sạch hơn, và các khiếm khuyết do làm đông-mô hoặc sấy khô (coagulation or desiccation defects) sẽ ít hơn; như vậy, cũng làm cho xét nghiệm giải phẫu bệnh được đơn giản hơn.
Ưu điểm chính của phẫu thuật cắt tuyến tiền liệt qua đường niệu đạo lưỡng-cực (bipolar TURP) là làm tăng độ an toàn cho bệnh nhân, bởi vì kỹ thuật này dùng dung dịch nước muối để tưới rửa, cho phép loại trừ được hội chứng cắt qua đường niệu đạo (TUR syndrome) và tình trạng giảm-natri huyết do loãng máu. Kỹ thuật này cũng cho phép cắt bỏ các tuyến tiền liệt có kích thước lớn, mà thời gian mổ thường cũng không bị hạn chế. Khi được sử dụng để cắt các khối u của bàng quang thì, với bộ dụng cụ lưỡng-cực, nguy cơ xảy ra phản xạ cơ bịt (obturator reflex) cũng giảm mạnh; bởi vì, hiệu ứng điện chỉ hạn chế ở nông, và còn cách xa bất kỳ lớp mô hoặc dây thần kinh nào ở sâu.
Trong phẫu thuật với bộ dụng cụ lưỡng-cực thì, chuyển động của quai dây kim loại hơi chậm hơn, so với dụng cụ của phẫu thuật cắt bỏ tuyến tiền liệt qua đường niệu đạo (TURP) chuẩn; nhưng, hiệu quả cầm máu lại có phần tốt hơn; từ đó, tổng thời gian mổ của hai phẫu thuật là gần như nhau. Mức độ chảy máu tổng thể trong- và sau-phẫu thuật, thời gian nằm viện, và tỷ lệ xảy ra biến chứng muộn, về cơ bản, cũng đồng nhất giữa hai công nghệ nói trên. Tuy nhiên cũng có các khó khăn sau đây: phải có một máy phát điện lưỡng-cực (bipolar generator), các quai dây kim loại được cải tiến đặc biệt để sử dụng thì hơi đắt hơn, so với các điện-cực là quai dây kim loại trong phẫu thuật cắt bỏ tuyến tiền liệt qua đường niệu đạo (TURP) chuẩn. Đặc biệt khi sử dụng bộ dụng cụ lưỡng-cực thì, cần có một máy làm ấm dịch tưới rửa, bởi vì, nó đảm bảo an toàn cho bệnh nhân, không những nhờ tác dụng ngăn ngừa giảm nhiệt độ cơ thể, vốn có thể xảy ra khi tiến hành phẫu thuật trong thời gian dài, mà còn bởi vì dung dịch nước muối ấm để tưới-rửa có tác dụng làm giảm thời gian chờ đợi giữa chừng (lag time), và cho phép cắt mô được nhanh hơn.
Bóc nhân tuyến tiền liệt bằng tia laser Holmium (Holmium enucleation of the prostate)
Kỹ thuật bóc nhân tuyến tiền liệt bằng laser Holmium, sử dụng năng lượng của tia laser holmium để cắt-gọt đi (carve out) hai thùy bên của tuyến này; kỹ thuật này chỉ là phiên bản nội soi của phẫu thuật bóc nhân mở. Khối mô được cắt ra, nói chung, thường quá lớn khó có thể lấy ra ngoài được qua một ống soi-cắt (resectoscope); do đó, lại phải đưa vào một dụng cụ cắt mô thành các mảnh nhỏ (tissue morcellator). Mới đầu, khối mô được cắt-gọt ra nổi lềnh bềnh ở trong bàng quang sẽ được bắt lấy, và dùng dụng cụ cắt-nhỏ để cắt ra nhỏ hơn; trong khi cắt, phải tránh không để dụng cụ cắt- nhỏ chạm vào thành của bàng quang. Phương pháp này cho phép cầm máu tốt và để lại được đủ lượng mô để đánh giá mô bệnh học. Tuy nhiên, kiểu can thiệp này về mặt kỹ thuật là rất thách thức, và rất tốn thời gian.
Theo các báo cáo so sánh giữa các kỹ thuật cắt bỏ tuyến tiền liệt khác nhau nói trên, do Van Melick và cs., Eaton và Francis, và Gilling và cs. đưa ra thì, tất cả các kỹ thuật này đều mang lại các cải thiện, mà đại để là, tương đương với phẫu thuật cắt bỏ tuyến tiền liệt qua đường niệu đạo (TURP) chuẩn về các mặt: chức năng tiểu tiện (urodynamics), số điểm theo thang đánh giá triệu chứng (symptom score), và các thông số đo lưu lượng nước tiểu (uroflowmetry parameters), trong vòng ít nhất 7 năm.
Noble và cs. cũng đã so sánh các kỹ thuật nói trên trong một thử nghiệm ngẫu nhiên có đối chứng theo một quan điểm kinh tế chặt chẽ. Các tác giả này kết luận rằng, các liệu pháp laser phi-tiếp xúc (noncontact laser therapies) có xu hướng là các lựa chọn điều trị ngoại khoa tốn phí nhất, trong khi phẫu thuật cắt bỏ tuyến tiền liệt qua đường niệu đạo (TURP) là biện pháp có hiệu quả-kinh tế (cost-effective) nhất.
5.3.3. Phương pháp phẫu thuật qua đường trên
• Chỉ định đối với u to > 50g, ( theo tài liệu khác > 75g).
• Những u phì đại có phối hợp với các bệnh lý khác: túi thừa bàng quang, sỏi, hoặc ở những bệnh nhân không đặt được máy nội soi…
• Hai phương pháp mổ được sử dụng là :
• Phương pháp Millin – phẫu thuật sau xương mu: Phẫu thuật này được Terrence Millin thực hiện lần đầu tiên vào năm 1945
Các bước phẫu thuật:
• Rạch da đường trắng giữa dưới rốn
• Bộc lộ mặt trước bàng quang và TLT
• Khâu cầm máu , mở mặt trước TLT
• Bóc tổ chức phì đại TLT, cầm máu cổ BQ
• Đặt sonde 3 chạc NĐ, khâu lại chỗ mở TLT.
• Phương pháp Hryntchak – phẫu thuật qua bàng quang.
• Mở vào BQ để bóc tổ chức phì đại TLT
• Đặt sonde NĐ và dẫn lưu BQ
5.4. Các phương pháp khác
Cắt nội soi với đường rạch từ cổ bàng quang tới ụ núi. Trong trường hợp bệnh nhân trẻ tuổi u phì đại nhỏ. Tuy nhiên những phương pháp này chưa được coi là phương pháp chuẩn vì nó không mang lại hiệu quả chắc chắn và triệt để.
• Nong niệu đạo TLT bằng bóng.
• Phương pháp điều trị bằng nhiệt.
• Sử dụng laser.
• Đặt các dụng cụ nòng trong niệu đạo TLT.
5.5. Điều trị tạm thời
• Trong trường hợp bệnh nhân bí tiểu cấp tính: cần đặt ống thông niệu đạo hoặc dẫn lưu bàng quang quang cấp cứu nếu không đặt được ống thông niệu đạo.
• Bệnh nhân suy thận: hai thận ứ nước do tắc nghẽn cổ bàng quang, nên dẫn lưu bàng quang để điều trị suy thận.
VI. Chăm sóc – Theo dõi sau mổ.
6.1. Chăm sóc theo dõi chung
Sau khi vừa trải qua cuộc phẫu thuật u xơ tiền liệt tuyến thì người nhà của người bị bệnh cần lưu ý tới sức khỏe của người bệnh nhằm có khả năng đảm bảo được cuộc giải phẫu đưa lại các hiệu quả tốt, tránh một số biến chứng nghiêm trọng có thể xảy ra, & Hỗ trợ cho việc hồi phục được nhanh hơn.
• Khi chăm chút người bệnh thì nên cho họ thời gian nghỉ ngời, đừng để người bị bệnh phải làm 1 số việc nặng nhọc, cần hạn chế đi lại, 1 số hoạt động mạnh để giữ cho vết thương không bị tổn thương, bị nhiễm trùng.
• Người nhà cần phải Hỗ trợ người bệnh luôn giữ được vệ sinh nhằm tránh nhiễm trùng xảy ra, cần phải thay băng thường xuyên cho người bệnh.
6.2 Chăm sóc đặc biệt
6.2.1. Rửa bàng quang liên tục
Sau mổ bóc u phì đại TLT hoặc cắt u qua nội soi đều phải rửa bàng quang liên tục. Mục đích tránh máu cục trong BQ và tắc ống dẫn lưu BQ.
Nước rửa thông thường dùng HTM 0,9% hoặc nước cất. Tốc độ dịch vào tuỳ thuộc tốc độ chẩy máu, nếu dịch ra có mầu hồng nhạt là được. Dịch rửa cần theo dõi liên tục, chỉ cần ngừng rửa vài phút có thể gây máu cục và tắc sonde BQ. Thời gian rửa tuỳ thuộc vào sự chẩy máu. Thông thường chẩy máu nhiều trong 24 giờ đầu, những ngày sau ít hơn và khoảng 3-4 ngày sau nước tiểu trong. Nếu máu chẩy nhiều có nguy cơ tắc sonde BQ phải bơm rửa BQ lấy máu cục.
6.2.2. Các biến chứng khác
Nhiễm khuẩn máu sau mổ: Biểu hiện Bn sốt rét run, huyết áp tụt < 90mmHg Cần cấy máu, cấy nước tiểu, báo phẫu thuật viên để hồi sức và cho KS thích hợp.
Hội chứng nội soi: TUR Syndrome (2%). Hội chứng nội soi là một biến
chứng do tái hấp thu nước rửa trong quá trình cắt nội soi TLT. Các nghiên cứu cho thấy lượng nước hập thu vào trong cơ thể mỗi phút là 20ml. Lượng nước hấp thu trong giờ đầu là 1000ml-1200ml. 1/3 số nước này hấp thu trực tiếp qua đường tĩnh mạch. Do nước hấp thu vào trong lóng mạch gây nên tình trạng hạ Na máu, gây phù tổ chức. Hậu quả là phù phổi, phù não, hôn mê, trụy tim mạch, tan máu, suy thận cấp và sốc.
Hội chứng nội soi xẩy ra khi lượng Na máu dưới 125 mEq.
Điều trị căn bản là phải nâng nồng độ Na máu. Lượng Na máu cần bù được tính theo công thức: Na+ = (140 – nồng độ Na hiện có) x 0,6 x trọng lượng cơ thể. 1 lít NaCl 9‰ chứa 154 mEq, 1 lít NaCl 3% chứa 815 mEq Na. Đồng thời sử dụng thuốc lợi tiểu để tăng đào thải nước và chống suy thận.
Chỉ định rút sonde niệu đạo sau mổ tuỳ thuộc phẫu thuật viên.
Đối với mổ nội soi thường sau 3-4 ngày. Đối với mổ đường trên sau 7-10 ngày. Khi rút sonde thường cho dịch rửa vào đầy BQ trước khi rút. Sau khi rút sonde, cho Bn đái đặt lại sonde tiểu đo lượng nước tiểu cặn và cấy vi khuẩn nước tiểu.
6.2.3. Biễn chứng muộn
Tỷ lệ chết : Rất thấp, thường liên quan đến các tai biến của kỹ thuật mổ.
Chảy máu sau mổ :
Chảy máu ngay lập tức sau mổ thường ít khi xảy ra. Đôi khi có chảy máu trong mổ.
Chảy máu muộn 10-20 ngày. Hay xảy ra sau mổ cắt u nội soi do bong các sẹo cầm máu sau mổ nội soi. Đa số tự cầm, đôi khi đòi hỏi đặt sonde bàng quang hút máu cục.
Đái khó sau mổ :
* Sớm : Thường liên quan đến viêm, phù nề cổ bàng quang đôi khi do kỹ thuật mổ. Nhất là mổ nội soi có thể cắt không hết u, cần phải can thiệp lại.
* Muộn : Xơ cứng, viêm dính xơ ổ TLT – -> can thiệp lại.
Hẹp niệu đạo sau mổ : Nong hoặc cắt trong niệu đạo .
• Trước mọi trường hợp đái khó sau mổ cần phải cảnh giác K TLT.
• Tái phát u sau 7-15 năm (7- 15%).
Đái rỉ sau mổ :
Chỉ nói đái rỉ thực thụ khi nó tồn tại sau mổ nhiều tháng (>6 tháng). Nguyên nhân do làm phá huỷ hệ thống cơ thắt vân niệu đạo. Rất ít xảy ra, Thường gặp sau mổ nội soi.
Điều trị :
Đặt cơ thắt nhân tạo.
Nhiễm trùng sau mổ :
Viêm mào tinh hoàn.
Viêm tắc tĩnh mạch – nhồi máu phổi :
Điều trị ngoại khoa u phì đại lành tính trở nên đơn giản và kết quả tốt, bệnh nhân nằm viện 5-10 ngày.
Tài liệu tham khảo :
1. Triệu chứng học Ngoại khoa . Nhà XB Y học 2000.
2. Ngoai khoa cơ sở Nhà XB Y học 2000.
3. Bệnh học tiết niệu Nhà XB Y học 2003.
4. Henry Gray (1821–1865). Anatomy of the Human Body
5. Prostate Hyperplasia, Benign. Last Updated: November 18, 2010